「人間ドックで膵臓に”のう胞”があると言われた」「IPMNの疑いで経過観察と言われたけれど、何を見ているの?」「このまま放っておいて大丈夫なのだろうか…」
こうした不安を抱えている方は少なくありません。膵のう胞は症状が出にくいため、検診や人間ドックで偶然見つかるケースが増えています。「経過観察」と言われても、その中身が分からなければ漠然とした不安だけが残ってしまうものです。
この記事では、IPMN(膵管内乳頭粘液性腫瘍)をはじめとする膵のう胞を指摘された方に向けて、以下の内容を消化器内科医の視点から解説します。
- IPMNの基礎知識と種類ごとのリスク
- 経過観察で医師が見ている具体的なポイント
- CT・MRIなど画像検査の役割と使い分け
- 専門医への紹介が必要なケース
- 経過観察の期間と終了の目安
まずは正しい知識を身につけ、必要な検査を適切なタイミングで受けていきましょう。
検診で「膵のう胞」「IPMN」を指摘されたら
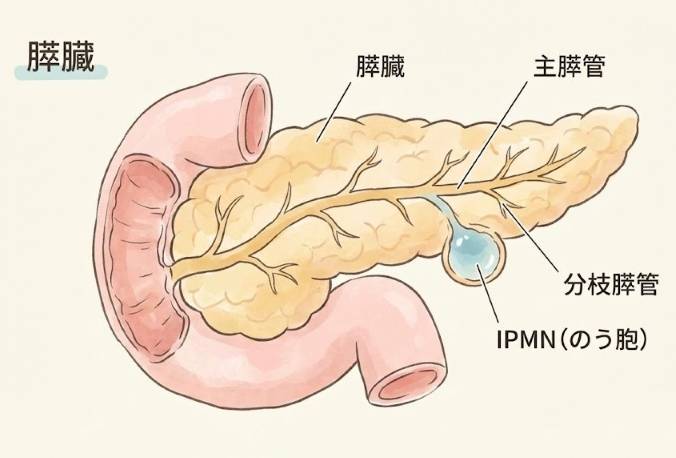
膵のう胞とは
膵のう胞とは、膵臓の中や周囲にできる液体を含んだ袋状の病変です。画像診断技術の進歩と健診の普及により、腹部超音波検査やCTで偶然発見される機会が大幅に増えました。
膵のう胞が見つかる頻度は検査方法や対象集団によって幅があり、健診の腹部超音波では0.2〜数%程度、MRIではさらに高い頻度で発見されるとの報告があります。
膵のう胞にはいくつかの種類があり、すべてが問題になるわけではありません。しかし、その中でも特に注意が必要なのがIPMN(膵管内乳頭粘液性腫瘍)です。
IPMNが見つかるきっかけ
IPMNは多くの場合、症状がないまま検診で発見されます。代表的な発見のきっかけには以下のようなものがあります。
- 人間ドックの腹部超音波検査
- 他の病気の精査で撮影したCTやMRI
- 健康診断での血液検査異常(膵酵素の軽度上昇など)をきっかけとした追加検査
【よくある相談パターン①】 「健診で膵臓にのう胞があると言われたけど、”経過観察”とだけ書かれていて、何をすればいいか分からない。」
このようなケースでは、まず消化器内科でのう胞の種類と大きさを正確に評価してもらうことが第一歩です。膵のう胞にはIPMN以外にも漿液性嚢胞腫瘍(SCN)や粘液性嚢胞腫瘍(MCN)など複数の種類があり、それぞれ経過観察の方針が異なります。
IPMNとは?種類と悪性化リスクの基礎知識
IPMNの定義
IPMN(Intraductal Papillary Mucinous Neoplasm:膵管内乳頭粘液性腫瘍)とは、膵管の内側に乳頭状の腫瘍ができ、粘液を産生することで膵管が拡張する病変です。この拡張した膵管がのう胞(袋状の病変)のように見えるため、「膵のう胞」として発見されることが多いです。
IPMNの多くは良性ですが、一部は時間をかけて悪性化(がん化)する可能性があります。そのため、国際診療ガイドライン(Kyoto Guidelines 2024)では定期的な経過観察が推奨されています。
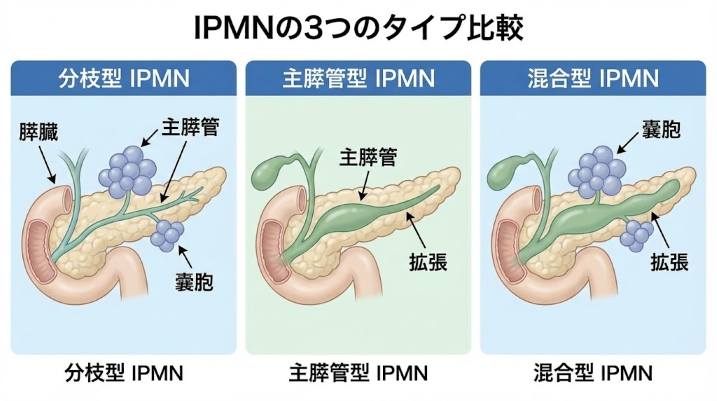
IPMNの3つのタイプ
IPMNは発生する場所によって3つのタイプに分類され、タイプによって悪性化リスクが異なります。
| タイプ | 特徴 | 悪性化リスク |
|---|---|---|
| 分枝型 | 膵管の枝(分枝膵管)にできる。ぶどうの房状に見えることが多い | 比較的低い |
| 主膵管型 | 膵液が流れる太い管(主膵管)にできる。主膵管全体が拡張 | 比較的高い |
| 混合型 | 分枝型と主膵管型の両方の特徴を持つ | 主膵管型に準じる |
検診で見つかるIPMNの多くは分枝型です。分枝型IPMNは良性のまま経過することが多いものの、長期間の経過で悪性化するケースもあるため、定期的なフォローアップが必要とされています。
膵がんとの関係
IPMNと膵がんの関係には、大きく分けて2つのパターンがあります。
- IPMN由来膵がん:IPMN自体ががん化するパターン
- IPMN併存膵がん:IPMNとは離れた場所に通常の膵がんが発生するパターン
分枝型IPMNにおける膵がんの発生頻度については報告によって差が大きく、数%〜10%程度とされる報告が多いですが、長期間の観察では累積発生率が10%を超える報告もあります。また、IPMN患者における膵がんの発生リスク(標準化罹患比:SIR)は、一般の方と比べて約15.8倍高いとする報告があります。
経過観察で医師が見ている3つのポイント
IPMNの経過観察は「ただ待つ」「様子を見る」という受動的なものではありません。国際診療ガイドラインでは、悪性化を示唆する”High-risk stigmata(高リスク所見)”と”Worrisome features(懸念所見)”が明確に定義されており、これらの有無を画像検査で定期的にチェックします。
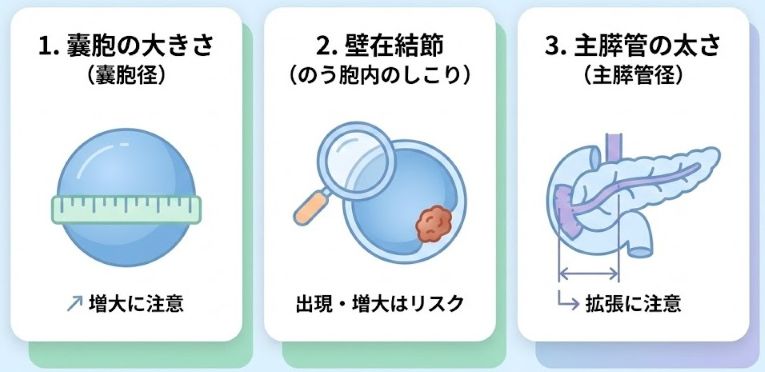
医師が見ている3つの主要ポイント
① のう胞の大きさと増大速度
のう胞(拡張した分枝膵管)の大きさは経過観察の重要な指標です。
- 3cm以上:精査が検討される目安(懸念所見)
- 年間2.5mm以上の増大:2024年のKyoto Guidelinesで追加された懸念所見
のう胞が大きいほど、また増大速度が速いほど、悪性化のリスクが高まる可能性があります。ただし、大きさだけで判断するのではなく、他の所見と総合的に評価します。
② 結節(壁在結節)の有無と大きさ
のう胞の内側にできる「こぶ」のような隆起を**壁在結節(へきざいけっせつ)**と呼びます。
- 5mm以上の造影される結節:高リスク所見(手術適応を検討)
- 5mm未満の結節:懸念所見として注意深く経過観察
結節は悪性化の重要なサインとされており、特に造影CTやMRIで「造影効果がある(血流がある)」結節は注意が必要です。
③ 主膵管の太さ
主膵管(膵液が流れるメインの管)の拡張も重要な指標です。
- 10mm以上:高リスク所見(手術適応を検討)
- 5〜9mm:懸念所見として精査を検討
主膵管の拡張は、IPMNが主膵管に及んでいる可能性や、膵液の流れが妨げられている可能性を示唆します。
その他のチェック項目
上記3つの主要ポイントに加えて、以下の項目も経過観察でチェックされます。
- 嚢胞壁の肥厚:壁が厚くなっていないか
- リンパ節の腫れ:膵臓周囲のリンパ節に異常がないか
- 糖尿病の新規発症・悪化:膵機能低下のサイン
- 血液検査(腫瘍マーカー):CA19-9などの値
【よくある相談パターン②】 「前回と比べてのう胞が少し大きくなったと言われて心配になった…」
のう胞は加齢とともにわずかに増大することもあります。1〜2mmの変化であれば測定誤差の範囲内であることも少なくありません。増大速度や他の所見と合わせて総合的に判断するため、1回の検査結果だけで過度に心配する必要はありません。次回の検査で変化の傾向を確認することが大切です。
CT・MRIなど画像検査それぞれの役割
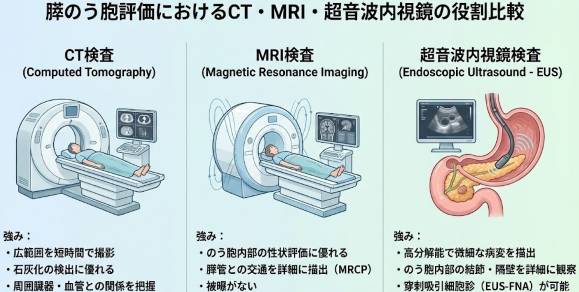
IPMNの経過観察では、複数の画像検査を使い分けます。それぞれに得意分野があり、必要に応じて組み合わせることで診断精度を高めます。
主な画像検査と特徴
造影CT
造影剤を使用して撮影するCT検査です。
得意なこと
- 結節の造影効果(血流の有無)の評価
- 膵臓全体の形態評価
- 周囲臓器やリンパ節の評価
- 短時間で撮影可能
注意点
- 放射線被ばくがある
- 造影剤アレルギーや腎機能低下がある方は注意が必要
MRI(MRCP)
磁気を利用した検査で、MRCP(MR胆管膵管撮影)は膵管・胆管を詳細に描出できます。
得意なこと
- 膵管との交通(のう胞が膵管とつながっているか)の確認
- のう胞内部の性状評価
- 主膵管の拡張や狭窄の評価
- 放射線被ばくがない
注意点
- 撮影時間がCTより長い
- 体内金属(ペースメーカーなど)がある方は制限あり
- 閉所恐怖症の方は相談が必要
超音波内視鏡(EUS)
胃や十二指腸から超音波プローブを挿入し、膵臓を至近距離から観察する検査です。
得意なこと
- CTやMRIで見えにくい小さな結節の検出
- 結節の詳細な形態評価
- 必要に応じて穿刺吸引(細胞や液体の採取)が可能
注意点
- 内視鏡検査のため、鎮静剤を使用することが多い
- 実施できる施設が限られる
- 検査医の技量に依存する部分がある
ガイドラインでの推奨
2024年のKyoto Guidelinesでは、MRI(MRCP)での経過観察が望ましいとされています。被ばくがなく、膵管の状態を詳細に描出できるためです。MRIで変化が認められた場合に、CTや超音波内視鏡を追加して詳しく評価するという流れが推奨されています。
ただし、ガイドラインには「画像診断法は医療機関の方針で変更可能」との記載もあり、実際には患者さんの状況や医療機関の設備に応じて検査方法が選択されます。
【よくある相談パターン③】 「毎回CTを受けているけど、被ばくが心配。MRIに変えてもらえますか?」
経過観察が長期にわたる場合、MRIを中心に据えることで累積被ばくを抑えられます。担当医に相談すれば、適切な検査スケジュールを一緒に考えてもらえます。ただし、MRIが受けられない事情(体内金属など)がある場合は、被ばく量を考慮しながらCTの間隔を調整するなどの対応も可能です。
専門医への紹介が必要なケースとは
かかりつけ医での経過観察中に、以下のような所見が出現・悪化した場合は、膵臓専門の医療機関での精査が検討されます。
高リスク所見(High-risk stigmata):手術適応を検討
以下の所見がある場合は、悪性(がん)の可能性が高いと考えられ、手術が検討されます。
- 造影される5mm以上の結節または固形成分
- 主膵管径が10mm以上
- 膵頭部病変による閉塞性黄疸(皮膚や白目が黄色くなる)
- 細胞診で悪性または悪性疑い
懸念所見(Worrisome features):精査が必要
以下の所見がある場合は、超音波内視鏡(EUS)などによる詳しい評価が推奨されます。
- のう胞径が3cm以上
- 造影されない結節
- 主膵管径が5〜9mm
- のう胞壁の肥厚や造影効果
- 主膵管径の急激な変化と膵萎縮
- リンパ節腫大
- CA19-9高値
- 年間2.5mm以上ののう胞増大
- 糖尿病の新規発症または急激な悪化
紹介が検討されるタイミング
【重要】 「所見がある=すぐに手術」ではありません。患者さんの年齢、全身状態、合併症、そして本人の希望なども踏まえて総合的に判断されます。
【よくある相談パターン④】 「結節があると言われたけど、すぐに手術しないといけないの?」
結節があっても、大きさや造影効果によっては経過観察が選択されることもあります。5mm未満の結節であれば、まずは超音波内視鏡で詳しく評価し、その結果を踏まえて方針を決めるケースが多いです。焦らず、専門医の評価を受けてから判断しましょう。
経過観察の期間・間隔と終了の目安
IPMNの経過観察は、多くの場合長期間にわたります。「いつまで続けるのか」「どのくらいの間隔で検査を受けるのか」は患者さんにとって大きな関心事です。
のう胞サイズ別の検査間隔(Kyoto Guidelines 2024)
2024年のKyoto Guidelinesでは、のう胞の大きさによって検査間隔が異なることが示されています。懸念所見がない分枝型IPMNの場合、おおむね以下のような目安が推奨されています。
| のう胞径 | 推奨される検査間隔 |
|---|---|
| 20mm未満 | 初回は6か月後に再検査→安定していれば18か月ごと |
| 20〜30mm | 初回は6か月後×2回→安定していれば12か月ごと |
| 30mm以上 | 6か月ごと(懸念所見として精査も検討) |
ただし、日本ではIPMN併存膵がん(IPMNとは別の場所にできる膵がん)のリスクも重視されており、のう胞サイズに関わらず6か月ごとの経過観察を行っている専門施設も少なくありません。具体的な検査間隔は担当医と相談して決めることが大切です。
経過観察の終了について
2024年のKyoto Guidelinesでは、経過観察の終了という選択肢が新たに示されました。これは以下のような背景があります。
- 生涯にわたる経過観察による患者さんの精神的・肉体的負担
- IPMN患者数の増加による医療側のキャパシティの問題
- 経過観察を続けても発見できない併存膵がんの存在
経過観察終了を検討できる条件
ガイドラインでは、以下の条件を満たす場合に経過観察の終了を「考慮してよい」とされています。
- のう胞径が20mm未満の小さな分枝型IPMN
- 5年間、変化がない
- 懸念所見がない
ただし、終了を決定する際には以下の点も考慮されます。
- 併存膵がんのリスク
- 患者さんの年齢と全身状態
- 余命の見込み
- 患者さん本人の希望
日本における考え方
【重要】 日本ではIPMN併存膵がんの問題が特に重視されており、「5年経ったから安心」とは考えない専門家が多いのが実情です。経過観察を終了するかどうかは、必ず担当医とよく相談して決めてください。
また、ガイドラインには「患者さんが手術に耐えられない場合や余命が限られている場合には、経過観察の中止を検討する」との記載もあります。これは、仮にがんが見つかっても治療できない状況では、検査を続ける意義が薄れるためです。
【よくある相談パターン⑤】 「何年も変化がないので、もう検査に行かなくても大丈夫ですか?」
自己判断で通院をやめることは推奨されません。変化がないことは良いサインですが、併存膵がんはIPMNの大きさに関係なく発生する可能性があります。検査の継続・終了は、担当医と相談のうえで判断しましょう。
まとめ
検診でIPMNや膵のう胞を指摘されると、「膵がんになるのでは」と不安になるのは自然なことです。しかし、多くのIPMN(特に分枝型)は良性のまま経過し、適切な経過観察を続けることで万が一の変化も早期に捉えることができます。
この記事のポイント
- IPMNは膵管にできる腫瘍で、分枝型・主膵管型・混合型の3タイプがある
- 経過観察では「のう胞の大きさ」「結節の有無」「主膵管の太さ」を定期的にチェック
- MRI(MRCP)を中心とした画像検査が推奨され、必要に応じてCTや超音波内視鏡を追加
- 高リスク所見があれば専門施設での精査・手術の検討を
- 検査間隔はのう胞の大きさによって異なり、担当医と相談して決める
- 経過観察の終了は慎重に判断し、必ず担当医と相談
受診の目安
| 状況 | 対応 |
|---|---|
| 検診で膵のう胞を指摘された | 消化器内科で精密検査を |
| 経過観察中で次回検査の案内が来た | 予定どおり受診を |
| 腹痛・背部痛・黄疸・急な体重減少がある | 早めに受診を |
| 糖尿病が新たに見つかった、または急激に悪化した | 早めに受診を |
| 何年も変化がなく、経過観察を続けるか迷っている | 担当医に相談を |
金沢・野々市・白山市エリアの方へ
膵のう胞やIPMNの経過観察について相談したい方は、消化器内科を受診いただくことで、画像評価や今後のフォロー方針についてご相談いただけます。当院(金沢消化器内科・内視鏡クリニック)でも腹部超音波検査やCTによる評価に対応しており、必要に応じてMRIや超音波内視鏡が可能な専門施設への紹介も行っています。
不安を抱え込まず、まずはお気軽にご相談ください。
▶ [当院のCT検査の詳細はこちら]
- IPMNはすべて膵がんになりますか?
-
いいえ、IPMNがすべて膵がんになるわけではありません。特に分枝型IPMNの多くは良性のまま経過します。膵がんの発生頻度は報告によって差がありますが、定期的な画像検査による経過観察を続けることで、変化があっても早期に発見できる可能性が高まります。
- 経過観察はどのくらいの間隔で受けるべきですか?
-
のう胞の大きさやリスク所見の有無によって異なります。Kyoto Guidelines 2024では、20mm未満で安定していれば18か月ごと、20〜30mmなら12か月ごと、30mm以上なら6か月ごとが目安とされています。担当医と相談のうえ、適切な間隔を決めましょう。
- CTとMRIはどちらが良いですか?
-
2024年のKyoto Guidelinesでは、MRI(MRCP)での経過観察が望ましいとされています。被ばくがなく、膵管の状態を詳しく描出できるためです。ただし、変化があればCTや超音波内視鏡を追加することもあります。どの検査が適切かは担当医と相談してください。
- 膵のう胞があると膵がんになりやすいのですか?
-
IPMNは膵がんのリスク因子とされています。IPMN患者における膵がんの発生リスク(標準化罹患比)は一般の方の約15.8倍との報告があります。リスクはゼロではありませんが、定期的な経過観察で早期発見につなげることが可能です。
- 経過観察中に症状が出たらどうすればいいですか?
-
腹痛、背部痛、黄疸(皮膚や白目が黄色くなる)、急な体重減少、糖尿病の新規発症や悪化などがあれば、次回の検査を待たずに早めに消化器内科を受診してください。これらはIPMN悪性化や併存膵がんを示唆する可能性があります。
- 経過観察を途中でやめても大丈夫ですか?
-
自己判断で中断することは推奨されません。最新の国際ガイドラインでは「20mm未満の小さな分枝型IPMNで5年間変化がない場合に終了を検討できる」とされていますが、日本ではIPMN併存膵がんのリスクも重視されています。終了の判断は必ず担当医と相談してください。
- 結節があると言われました。すぐに手術ですか?
-
結節があっても、すぐに手術とは限りません。結節の大きさや造影効果によって対応が異なります。5mm以上の造影される結節は手術適応を検討しますが、小さな結節は超音波内視鏡で詳しく評価してから判断することが多いです。焦らず専門医の評価を受けましょう。
- どこで経過観察を受ければいいですか?
-
消化器内科のあるクリニックや病院で経過観察が可能です。必要に応じてMRIや超音波内視鏡が可能な専門施設への紹介も受けられます。金沢・野々市・白山市エリアでは当院でもCTや超音波検査による初期評価に対応しており、専門施設への紹介体制も整えています。
参考文献
- International evidence-based Kyoto guidelines for the management of intraductal papillary mucinous neoplasm of the pancreas
Ohtsuka T, Fernández-del Castillo C, Furukawa T, et al. Pancreatology. 2024;24(2):255-270. doi: 10.1016/j.pan.2023.12.009 - The Revised Kyoto Criteria and Risk of Malignancy Among Patients With Intraductal Papillary Mucinous Neoplasms
Hamada T, et al. Clinical Gastroenterology and Hepatology. 2024. doi: 10.1016/j.cgh.2024.05.043 - Surveillance for Presumed BD-IPMN of the Pancreas: Stability, Size, and Age Identify Targets for Discontinuation
Marchegiani G, et al. Gastroenterology. 2023. doi: 10.1053/j.gastro.2023.06.022 - Long-Term Outcomes and Risk of Pancreatic Cancer in Intraductal Papillary Mucinous Neoplasms
de la Fuente J, et al. JAMA Network Open. 2023;6(10):e2337799. doi: 10.1001/jamanetworkopen.2023.37799 - Factors associated with the risk of progression of low-risk branch-duct intraductal papillary mucinous neoplasms
Capurso G, Crippa S, Vanella G, et al. JAMA Network Open. 2020;3(11):e2022933. doi: 10.1001/jamanetworkopen.2020.22933 - Long-term risk of malignancy in branch-duct intraductal papillary mucinous neoplasms
Oyama H, Tada M, Takagi K, et al. Gastroenterology. 2020;158(1):226-237.e5. doi: 10.1053/j.gastro.2019.08.032 - European evidence-based guidelines on pancreatic cystic neoplasms
European Study Group on Cystic Tumours of the Pancreas. Gut. 2018;67(5):789-804. doi: 10.1136/gutjnl-2018-316027 - Incidence of synchronous and metachronous pancreatic carcinoma in 168 patients with branch duct intraductal papillary mucinous neoplasm
Tanno S, et al. Pancreatology. 2010;10(2-3):173-178. doi: 10.1159/000231982 - 膵癌診療ガイドライン 2022年版(日本膵臓学会)










